Quotient de réaction
Introduction
-
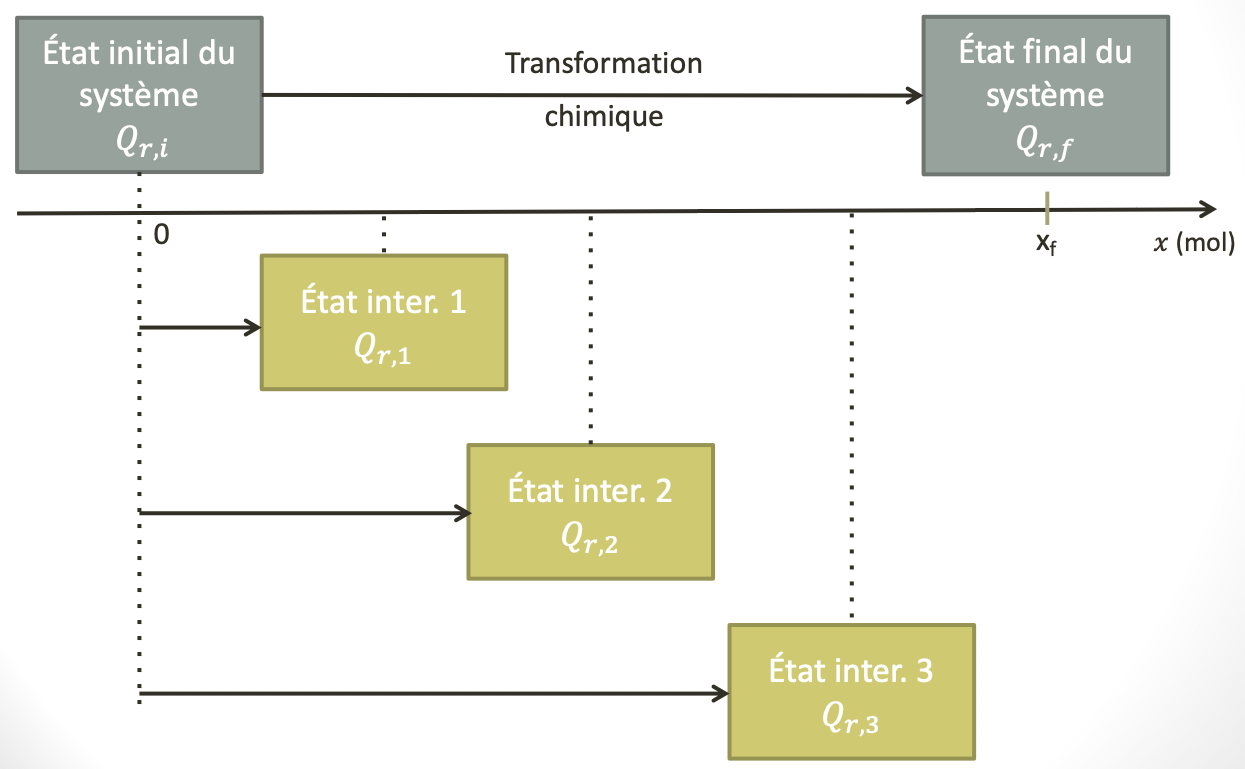
Le quotient de réaction $Q_r$ est une grandeur qui caractérise un système chimique dans un état donné.
-
L’évolution de sa valeur au cours de la transformation renseigne sur l’évolution du système chimique étudié.
Le quotient de réaction calculé dans deux états différents du système aura deux valeurs différentes à moins que ces deux états ne soient des états d’équilibre.
Expression de $Q_r$ dans le cas de systèmes chimiques uniquement constitués d’espèces dissoutes
Le quotient de réaction $Q_r$ de la réaction d’équation chimique
$$
\ce{ \alpha{} A (aq) + \beta B (aq) <=> \gamma C (aq) + \delta D (aq)}
$$
a pour expression, lorsque toutes les espèces sont dissoutes dans la solution
$$
Q_r = \dfrac{\left( \dfrac{[{C}]}{C^o} \right)^\gamma \cdot \left( \dfrac{[{D}]}{C^o} \right)^\delta}{\left( \dfrac{[{A}]}{C^o} \right)^\alpha \cdot \left( \dfrac{[{B}]}{C^o} \right)^\beta}
$$
avec $C^o = \pu{1,00 mol.L-1}$.
$Q_r$ est une grandeur sans dimension.
Soit l’équation de la réaction d’oxydation des ions thiosulfate $\ce{S2O3^{2-}}$ par le diiode $\ce{I2}$. Il se forme des ions tetrathionate $\ce{S4O6^{2-}}$ et des ions iodure $\ce{I-}$.
[Lire]
Équilibre Chimique
Publié le January 7, 2021
| 10 minutes
| 2081 mots
|
Action du chlorure d’hydrogène sur l’eau
On introduit $\pu{0,010 mol}$ de chlorure d’hydrogène $\ce{HCl (g)}$ dans $\pu{1,0 L}$ d’eau. On mesure le pH de la solution ainsi formée et on obtient : $\mathrm{pH} = \pu{2,0}$.
On fait l’hypothèse que la transformation de dissolution est totale.
- La transformation due à la réaction chimique entre le chlorure d’hydrogène solubilisé et l’eau est-elle totale ?
Solution
$$
\ce{HCl (aq) + H2O –> Cl^- (aq) + H3O^+}
$$
[Lire]
