Documents
Bétadine
La Bétadine® dermique 10% est un antiseptique et désinfectant à base d’iode, indiqué pour le nettoyage des plaies ou brûlures superficielles et peu étendues. La Bétadine® peut être utilisée pure, en badigeonnage sur la peau, ou diluée avec de l’eau ou du sérum physiologique pour le lavage et l’irrigation des plaies.Les agents à visée antiseptique ne sont pas stérilisants : ils réduisent temporairement le nombre de micro-organismes.
[Lire]Dosage d'un antiseptique : l'eau de Dakin
Documents
Eau de Dakin

La liqueur de Dakin (eau de Dakin) est une solution antiseptique utilisée pour le lavage des plaies et des muqueuses, de couleur rose et à l’odeur d’eau de Javel. Elle a pour avantage de ne pas être colorante (contrairement à l’éosine, par exemple) et de ne pas produire de sensation d’irritation à l’usage (contrairement à la Bétadine par exemple).
Lors de la Première Guerre mondiale, le chimiste d’origine britannique, installé aux États-Unis, Henry Drysdale Dakin met au point avec le chirurgien français Alexis Carrel un antiseptique (dont la substance active est l’eau de Javel) pour les plaies ouvertes ou infectées, dans le cadre des travaux de ce dernier sur le traitement des plaies de guerre.
[Lire]Détermination de la composition d'une solution colorée, loi de Beer-Lambert
Il est assez facile de calculer la concentration massique ou la concentration molaire lorsqu’on sait comment la solution a été préparée : il suffit de diviser la masse (ou la quantité de matière) de soluté apporté par le volume du solvant1.
Mais comment déterminer la concentration en soluté apporté d’une solution que l’on n’a pas préparé ? Comment vérifier la valeur de la concentration en soluté apporté d’une solution ?
Ce chapitre introduit une méthode permettant de répondre à ces questions à la condition que la solution soit colorée !
[Lire]
Utiliser le réseau téléphonique pour surfer sur Internet
Documents
Affaiblissement des signaux
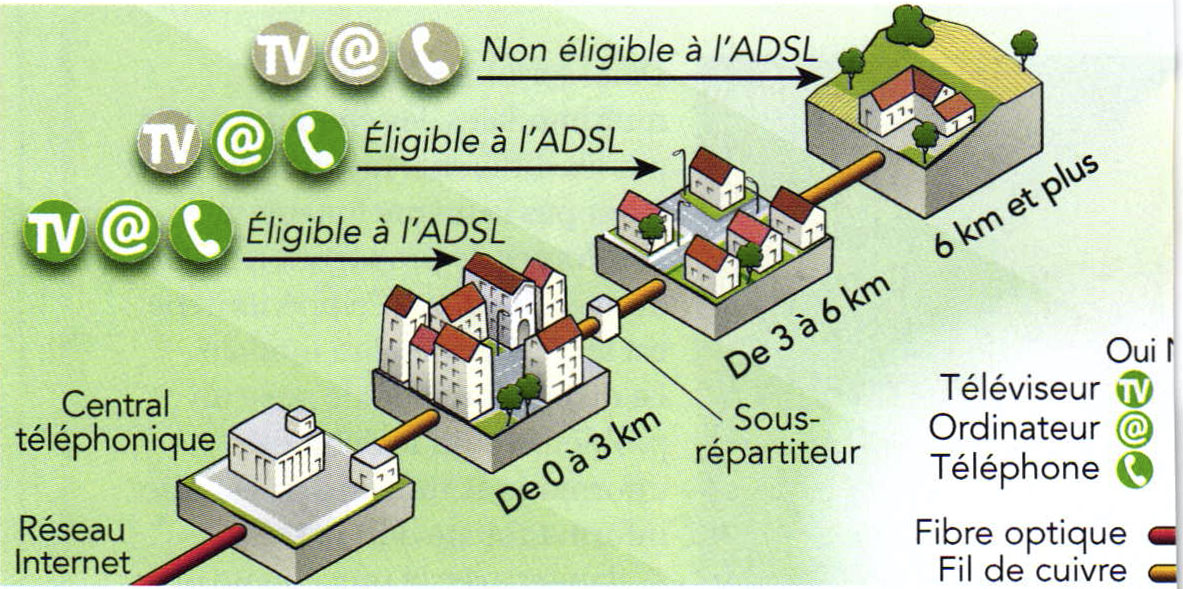
« Un courant électrique passant au travers d’un conducteur dissipe une partie de son énergie sous forme de chaleur (pertes par effet Joule). Il en résulte une diminution de la puissance de ce signal. Les pertes augmentent avec la résistance du câble. La résistance est elle-même fonction de la longueur du câble, de son diamètre et de sa résistivité1 […] Les technologies xDSL2 font passer des signaux électriques à haute fréquence dans les câbles téléphoniques, constitués de fils de cuivre. Compte tenu de ces hautes fréquences, un effet de peau3 apparaît ; il a pour conséquence d’augmenter fortement la résistance du câble, et donc d’atténuer d’autant plus le signal utile en raison du phénomène décrit précédemment. […] Il découle de ce phénomène que certaines habitations, proches des centraux téléphoniques […] bénéficient de débits élevés (jusqu’à $\pu{20 Mbit/s}$, permettant un grand confort d’usage et des services innovants tels que la télévision par ADSL), tandis que d’autres plus éloignés doivent se contenter de $\pu{512 kbit/s}$ — et ce pour un prix d’abonnement identique. »
[Lire]Évaluer l'atténuation du signal dans une fibre optique
Exercice
La puissance lumineuse d’un signal transmis par une fibre optique décroît avec la distance qu’il parcourt.
Le coefficient d’atténuation linéique $\alpha$ caractérise cette décroissance. ll est défini par la relation : $$ \alpha = \dfrac{10}{L} \, \log \left( \dfrac{ \cal I_e }{ \cal I_s } \right) $$ $\alpha$ est exprimé en décibel par unité de longueur ($\pu{dB/m}$), $L$ est la longueur de la fibre en mètre, $\cal I_e$ et $\cal I_s$ sont respectivement les intensités en entrée et en sortie du signal.
[Lire]Détermination de la composition d'une solution colorée, loi de Beer-Lambert
À ce stade de l’année, nous connaissons les grandeurs « concentration massique » et « concentration molaire ». Il est assez facile de calculer leur valeur lorsqu’on sait comment la solution a été préparée : il suffit de diviser la masse (ou la quantité de matière) de soluté apporté par le volume du solvant1.
Mais comment déterminer la concentration en soluté apporté d’une solution que l’on n’a pas préparé ? Comment vérifier la valeur de la concentration en soluté apporté d’une solution ?
[Lire]
Exercices du chapitre (Livre Scolaire)
Concentrations molaires et dilution
Exercice 1 : Solution de réhydratation
On peut effectuer des injections de solution aqueuse de fructose, de formule $\ce{C6H12O6}$, pour prévenir la déshydratation. De telles solutions sont obtenues en dissolvant une masse $m = \pu{25,0 g}$ de fructose pour $\pu{500 mL}$ de solution finale.
-
Déterminer la quantité de matière de fructose correspondant à la masse indiquée dans l’énoncé.
-
En déduire la concentration molaire de ces solutions en fructose.
[Lire]
Le design Culinaire
Situation expérimentale sur le site du Livre Scolaire (hors questions)
Images du montage expérimental
Solution d’extrait de choux rouge
Échelle de teinte
Montage expérimental avec spectrophotomètre
Exploitation des données
-
Télécharger le logiciel Spectral Analysis du fabriquant Vernier. Il existe des versions pour tous les systèmes d’exploitations.
-
Télécharger les fichiers résultats suivants (clic droit et enregistrer) et les ouvrir à tour de rôle à l’aide du logiciel juste téléchargé :
[Lire]
Composition Chimique des Solutions
Concentrations massique et molaire
Qu’est-ce qu’une solution ?
Exercice
On réalise une solution aqueuse de permanganate de potassium en introduisant $m = \pu{0,79 g}$ de permanganate de potassium solide, $\ce{KMnO4}$, dans $V_{0} = \pu{250 mL}$ d’eau distillée. On note $(S_0)$ cette solution et on suppose que la dissolution s’effectue sans effet de volume.
- Le permanganate de potassium est le soluté. Qu’est-ce cela signifie ?
Réponse
Un soluté est une espèce chimique ou un ensemble d’espèces chimiques que l’on dissout dans un solvant.
La quantité de matière d’un soluté est très inférieure à la quantité de matière du solvant.


